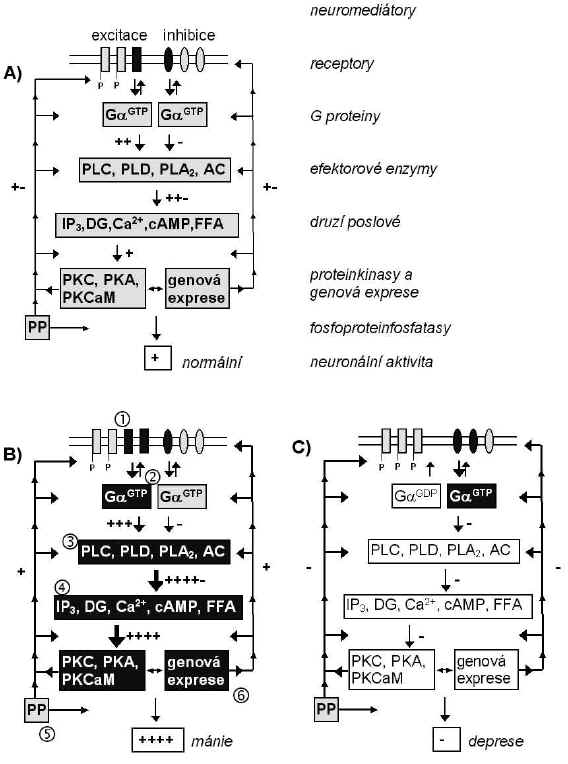
Postreceptorové hypotézy afektivních poruch vycházejí ze skutečnosti, že přenos nervového signálu může být ovlivněn i řadou jiných procesů než je dostupnost neuromediátoru v synaptické štěrbině nebo počet či afinita postsynaptických receptorů. Obecný model pro bipolární afektivní poruchu se zahrnutím těchto procesů je znázorněn na Obr. 4. Excitace a inhibice se v tomto modelu chápe obecně, tedy nejen jako signály vzniklé přímou aktivací různých receptorových systémů, ale jako libovolné procesy (endokrinní, farmakologické, vlivy chování nebo vnějšího prostředí apod.), jejichž výsledkem je za normálních podmínek určitá rovnováha excitačních a inhibičních signálů v mozku. Uvedený model vychází z obecně přijímaného předpokladu, že v manické fázi převažují určité excitační mechanismy nad inhibičními, zatímco v depresivní fázi je tomu naopak.
A) Normální přenos signálu
Neuromediátor se váže k receptoru a aktivuje tak G protein, který aktivuje či inhibuje efektorové enzymy a iontové kanály; tím dochází k následné změně koncentrací druhých poslů, které jsou schopny aktivovat proteinkinasy. Aktivované proteinkinasy umožňují fosforylaci enzymů, iontových kanálů, G proteinů a receptorů, mění tak jejich vlastnosti, což vede např. k depolarizaci či hyperpolarizaci membrány. Fosfoproteiny jsou substrátem pro fosfatasy, které je vracejí do původního stavu. Jak proteinkinasy, tak fosfatasy mohou zpětnovazebně ovlivňovat výše popsaný převod signálu. Za normálních podmínek existuje určitá rovnováha mezi excitačními a inhibičními systémy.
B) Manická fáze
Předpokládá se, že v manické fázi dochází k poruše této rovnováhy zvýšením excitačního přenosu, které je umožněno např. 1) zvýšením počtu a/nebo afinity excitačních receptorů při dostatku neuromediátoru; 2) snížením GTPasové aktivity Gas podjednotek; 3) zvýšením aktivity efektorových enzymů, např. PLC; 4) delší dobou života druhých poslů způsobenou snížením aktivity příslušných enzymů, např. fosfodiesterasy štěpící cAMP; 5) delší dobou života fosfoproteinů (v důsledku nedostatečné funkce fosfatasy), které zvyšují neuronální aktivitu; 6) zvýšenou genovou expresí aktivujících složek přenosového systému. Vliv může mít také změněná aktivita proteinkinas a enzymů podílejících se na syntéze, exocytoze a degradaci neuromediátorů.
Biochemické děje provázející manickou fázi mohou vést ke zvýšené fosforylaci receptorů aktivovanými proteinkinasami a/nebo ke snížení afinity receptorů v důsledku snížené GTPasové aktivity Ga. Zvýšený excitační přenos však trvá po dobu, kdy přetrvává zvýšená aktivace G proteinů, systémů druhých poslů nebo dalších složek. Jedná se o přechodné období před normalizací stavu, nebo před přesmykem do depresivní fáze.
C) Depresivní fáze
Snížení neuronální aktivity v depresivní fázi lze vysvětlit opačnými změnami v jednotlivých stupních přenosu signálu, než je uvedeno u manické fáze.
Střídání manické a depresivní fáze při bipolární afektivní poruše lze vysvětlit např. tak, že je aktivován systém, který způsobuje nejprve zvýšení neuronální aktivity a poté její snížení přes záporné zpětnovazebné mechanismy působící jak na vlastní, tak na jiné přenosové systémy.

Obr. 4: Obecný model pro bipolární afektivní poruchu