Receptor je makromolekula specializovaná na přenos informace. Je definován jako vazebné místo s funkčními vztahy. Funkčními vztahy se při synaptickém přenosu nervového signálu rozumí procesy, které jsou vyvolány vazbou neuromediátoru nebo jeho agonisty a které vedou ke změně propustnosti synaptické membrány pro určité ionty. Receptory lze dělit na cytoplasmatické, organelové a membránové (226). V receptorových hypotézách afektivních poruch se uvažují především membránové receptory, jejichž typy a podtypy jsou obvykle určovány na základě odlišných farmakologických profilů. Aktivace synaptických receptorů vede k otevření nebo uzavření určitých iontových kanálů, které mohou být 1) součástí receptoru (např. GABAA, nikotinový acetylcholinový, glutamátové ionotropní, 5-HT3, glycinový receptor); 2) regulovány přímo aktivovanými a podjednotkami G proteinů (např. adrenergní a2A, a2B, dopaminové D2, serotoninové 5-HT1A, GABAB receptory); 3) regulovány prostřednictvím systémů druhých poslů aktivovaných G proteiny, přičemž tato regulace může být přímá, nebo přes fosforylaci proteinů (např. b-AR, muskarinové acetylcholinové receptory, atd.).
Interakce neuromediátoru se specifickým receptorem nastává na jednom nebo více aktivních (specifických) rozpoznávacích místech a vede k aktivaci receptorového systému. Různá léčiva soutěží s neuromediátorem o obsazení těchto rozpoznávacích míst - jedná se o kompetitivní látky. Působení některých psychofarmak může být úplně, nebo částečně identické jako u fyziologického ligandu; hovoříme o úplných, nebo parciálních (částečných) agonistech. Podobně u inhibitorů mluvíme o úplných, nebo parciálních antagonistech. Při plně kompetitivní inhibici se inhibitor (úplný antagonista) váže na totéž vazebné místo jako neuromediátor, ale nedochází k aktivaci receptorového systému. Při parciálně kompetitivní inhibici se inhibitor (parciální antagonista) váže na místo blízké vazebnému místu neuromediátoru, čímž snižuje afinitu pro neuromediátor. Analogicky s enzymovou kinetikou lze reverzibilní inhibici nebo aktivaci receptorových systémů vztaženou k rozpoznávacím místům pro neuromediátory rozdělit do řady dalších typů.
Nehledě ke kompetici, vytvářejí některé látky ireverzibilní vazby
se skupinami v rozpoznávacích místech - jsou označovány jako blokátory.
Látky, které se vážou k vazebným místům na receptorovém komplexu
tak, že nedochází ke kompetici s neuromediátorem, jsou označovány
jako nekompetitivní. Konformační změny vyvolané vazbou nekompetitivních
látek však mohou ovlivnit jak vazbu neuromediátoru k receptoru, tak přenos
signálu o jeho vazbě. V mnoha případech jsou vazebná místa lokalizována
v místech kontaktu proteinového receptoru a fosfolipidové dvojvrstvy a
mohou být obsazována molekulami rozpustnými v lipidech. Změny ve
fosfolipidové dvojvrstvě (např. změny fluidity nebo změny lipidového složení)
proto mohou modifikovat aktivaci receptorového systému.
Receptory mohou relativně rychle měnit své vlastnosti a dostupnost (227). Regulace změnou počtu receptorů v odezvě na dlouhodobou (hodiny, dny) fyziologickou stimulaci zahrnuje jednak snížení (downregulaci) či zvýšení (upregulaci) celkového počtu receptorových vazebných míst pro agonisty, jednak relativně rychlejší reversibilní zanořování receptorů do cytoplasmy (sekvestraci). Snížení počtu receptorů může být způsobeno snížením poločasu života receptoru nebo ovlivněním exprese cílových genů. Regulace vlastností receptorů znamená změnu výsledné odezvy na stimulaci receptoru; tato odezva může být ovlivněna také vzájemnými vztahy mezi různými receptorovými systémy.
Často je však rozlišování uvedených dvou typů regulace nedůsledné, což se projevuje např. v používání pojmu desenzibilizace. Desenzibilizací receptoru se rozumí časné (během minut) snížení odezvy na interakci agonisty s receptorovým vazebným místem a patří tedy mezi regulace vlastností receptoru. Někteří autoři chápou desenzibilizaci obecněji a zahrnují do ní další děje vedoucí ke snížení biochemické odezvy na aktivaci receptoru. Mezi základní mechanismy desenzibilizace potom patří: 1) změny ve spojení podjednotek aktivních molekul vlivem fosforylace, ribosylace, změn membránových fosfolipidů, interakce arrestinů s receptory, atd.; 2) tvorba poslů, kteří aktivují látky působící inhibičně na receptor; 3) tvorba receptorových shluků nebo jejich rozptylování (zprostředkované cytoskeletem); 4) internalizace receptorů (endocytozou). Homologní desenzibilizace vzniká obvykle při kontinuálním vystavení receptoru jeho mediátoru nebo látce specificky interagující s tímto receptorem. Fosforylace receptorů je v tomto případě spojena jak s jejich funkčním odpojením z přenosového systému, tak s jejich odstraněním z buněčného povrchu. Heterologní desenzibilizace může vzniknout při interakci aktivních látek s molekulami aktivovanými v některé přenosové cestě, např. se systémem druhých poslů; funkce receptorů je regulována jejich fosforylací, ale nedochází k regulaci snížením počtu.
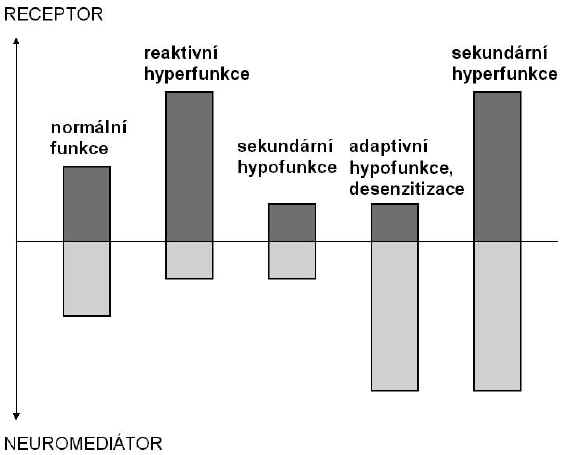
Jak již bylo uvedeno jsou receptory dynamické systémy, které se mohou přizpůsobovat a vyrovnávat tak např. změny v neuromediátorových systémech. Přizpůsobení (adaptace) receptorů zahrnující především regulaci změnou počtu receptorů může vést k těmto základním jevům (Obr. 5): 1) reaktivní (kompenzační) hyperfunkce, tj. zvýšení počtu receptorů jako kompenzace nedostatečné buněčné odezvy způsobené snížením dostupnosti neuromediátoru (předpokládá se např. při depresivní poruše); jedná se o základ hypersenzitivity, která se může projevit, když se obnoví dostupnost neuromediátoru při zvýšené hustotě receptorů (např. při přesmyku do manické fáze u bipolární afektivní poruchy); 2) sekundární hypofunkce vzniká, když při nedostatku určitého neuromediátoru dojde k současnému snížení počtu odpovídajících receptorů (např. při Alzheimerově, Huntingtonově nebo Parkinsonově chorobě); 3) adaptivní hypofunkce vzniká při nadměrném nebo častém uvolňování (hyperaktivitě) určitého neuromediátoru; dochází obvykle jak ke snížení počtu receptorů, tak jejich schopnosti vyvolat odpověď na stimulaci; 4) sekundární hyperfunkce, tj. paradoxní zvýšení denzity receptorů v odezvě na nadbytek neuromediátoru; nastává v určitých fázích některých onemocnění (např. při schizofrenii), při intoxikaci léky (např. amfetaminy) a byla pozorována i experimentálně (2).
Receptorové hypotézy afektivních poruch předpokládají, že s onemocněním a jeho léčbou jsou spojeny hlavně změny v monoaminových receptorech. Jejich receptorové komplexy většinou zahrnují tři složky: 1) rozpoznávací místo, ke kterému se specificky váže látka, na níž je receptor citlivý; 2) transdukční prvek (G protein), který přenáší a zesiluje signál o navázání aktivující látky; 3) efektorový systém (adenylátcyklasový, guanylátcyklasový, fosfoinositidový, iontové kanály řízené aktivovanými G proteiny), který zajišťuje buněčnou odezvu. Známé podtypy monoaminových receptorů spolu s transdukčními prvky a hlavními efektory jsou uvedeny v Tabulce 4; uvedeny jsou pouze receptory zjištěné u savců, u nichž byla většinou již potvrzena jejich endogenní exprese (podle TiPS Receptor and Ion Channel Nomenclature Supplement 1997).
Funkce a význam receptorových podtypů jsou určeny jednak lokalizací receptorů na daném neuronu, jednak jejich lokalizací v různých mozkových strukturách. Presynaptické somatické autoreceptory jsou lokalizovány na buňkách, které obsahují stejný neuromediátor, kterým jsou aktivovány. Postsynaptické heteroreceptory jsou lokalizovány na buňkách, které obsahují jiný neuromediátor, než kterým jsou aktivovány.
V mozku jsou b1-AR lokalizovány hlavně na neuronech, zatímco b2-AR jsou převážně na jiných typech buněk, např. na gliích. Stimulace b-AR vede k depolarizaci membrány, tj. ke zvýšení elektrické aktivity buňky v místě jejich lokalizace. a1-AR jsou lokalizovány především postsynapticky, a2-AR postsynapticky a malá část i presynapticky.
Změny v 5-HT receptorech byly při depresi a její léčbě pozorovány především u podtypů 5-HT1A a 5-HT2. 5-HT1A receptory se vyskytují v mozku jako presynaptické somatické autoreceptory, nebo jako postsynaptické heteroreceptory. Afinita 5-HT1A receptorů pro 5-HT je velmi vysoká. Jejich stimulace vede k hyperpolarizaci membrány, tj. ke snížení elektrické aktivity buňky. 5-HT2 receptory jsou lokalizovány hlavně v mozkové kůře a jsou to heteroreceptory; jejich stimulace vede k depolarizaci membrány.

Obr. 5: Adaptace receptorů
Tabulka 4
Podtypy monoaminových receptorů
|
RECEPTORY |
nomenklatura |
transdukční prvek |
hlavní efektor |
|
a1-adrenoceptory |
a1A |
Gq/11 |
IP3/DG |
|
|
a1B |
Gq/11 |
IP3/DG |
|
|
a1D |
Gq/11 |
IP3/DG |
|
a2-adrenoceptory |
a2A |
Gi/o |
cAMP¯, K+(G), Ca2+¯(G) |
|
|
a2B |
Gi/o |
cAMP¯, Ca2+¯(G) |
|
|
a2C |
Gi/o |
cAMP¯ |
|
b-adrenoceptory |
b1 |
Gs |
cAMP |
|
|
b2 |
Gs |
cAMP |
|
|
b3 |
Gs (Gi/o) |
cAMP |
|
dopaminové |
D1 |
Gs |
cAMP |
|
|
D2 |
Gi/o |
cAMP¯, K+(G), Ca2+¯(G) |
|
|
D3 |
Gi/o |
cAMP¯ |
|
|
D4 |
Gi/o |
cAMP¯ |
|
|
D5 |
Gs |
cAMP |
|
5-hydroxytryptaminové |
5-HT1A |
Gi/o |
cAMP¯, K+(G) |
|
|
5-HT1B |
Gi/o |
cAMP¯ |
|
|
5-HT1D |
Gi/o |
cAMP¯ |
|
|
5-HT1E |
Gi/o |
cAMP¯ |
|
|
5-HT1F |
Gi/o |
cAMP¯ |
|
|
5-HT2A |
Gq/11 |
IP3/DG |
|
|
5-HT2B |
Gq/11 |
IP3/DG |
|
|
5-HT2C |
Gq/11 |
IP3/DG |
|
|
5-HT3 |
vnitřní kationtový kanál (Na+/K+/Ca2+) |
|
|
|
5-HT4 |
Gs |
cAMP |
|
|
5-HT5A |
? |
|
|
|
5-HT5B |
? |
|
|
|
5-HT6 |
Gs |
cAMP |
|
|
5-HT7 |
Gs |
cAMP |
IP3 - inositol-1,4,5-trisfosfát; DG - sn-1,2-diacylglycerol; cAMP - cyklický adenosinmonofosfát; G - G protein, (G) - G protein podílející se na otevření nebo uzavření iontového kanálu; 5-HT - serotonin; (¯) - zvýšení (snížení) koncentrace druhého posla, nebo otevření (uzavření) iontového kanálu
Pozn.:
1) Serotoninové receptory byly původně rozděleny do podtypů 5-HT1 a 5-HT2 podle afinity k agonistům (5-HT1 s vysokou afinitou k serotoninu, 5-HT2 s vysokou afinitou ke spiperonu a ketanserinu). 5-HT1C byl později přejmenován na 5-HT2C; lidské 5-HT1Db a krysí 5-HT1B jsou nyní označovány společně jako 5-HT1B ; jako 5-HT1D jsou brány původní 5-HT1Da; 5-HT1E, 5-HT1F, 5-HT5A, 5-HT5B a 5-HT6 byly pouze klonovány (zatím nebyla nalezena jejich endogenní exprese).
2) Bylo zjištěno, že klonovaný a1C-adrenoceptor odpovídá farmakologicky definovanému a1A-adrenoceptoru.