Mnoho základních buněčných procesů, včetně zpracování informací, nitrobuněčného a mezibuněčného přenosu signálu, se odehrává v plazmatických membránách nebo jiných membránových strukturách. V této kapitole jsou uvedeny pouze základní informace o stavbě a vlastnostech membrán s ohledem na jejich funkci při šíření nervového signálu.
Biomembrány jsou tenké vrstvy oddělující buňku nebo její části od okolního prostředí. Jsou tvořeny vhodně uspořádanými lipidy a proteiny s malým množstvím vázaných cukrů. Jejich funkce spočívá v aktivní regulaci složení nitrobuněčného prostředí. Plazmatická membrána ohraničuje celou buňku, další membrány vymezují řadu organel eukaryot (jádro, mitochondrie, endoplazmatické retikulum, Golgiho aparát, synaptické váčky atd.).
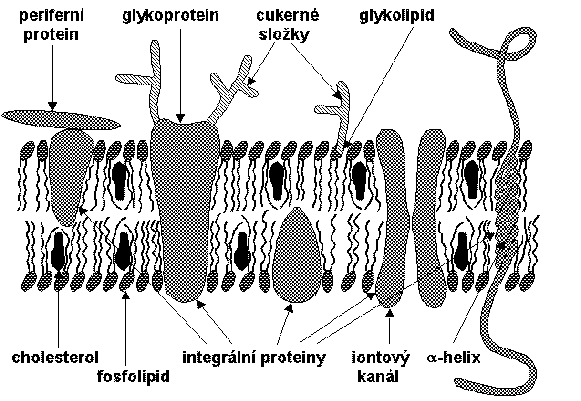
Buněčné membrány jsou tvořeny především lipidy, steroly, proteiny, glykolipidy a glykoproteiny. Mají jednotný organizační princip, tj. uspořádání většiny membránových lipidů do dvojné vrstvy (o tloušťce kolem 6 nm) s více či méně zanořenými proteiny. Poměr lipidů, proteinů a cukrů (vázaných v glykolipidech a glykoproteinech) se u různých membrán velmi liší. Lipidy tvoří 24% (ve vnitřní membráně mitochondrií) až 79% (v myelinové pochvě), proteiny 18% až 76% a cukry 2% až 10% z celkové hmotnosti membránových molekul. Lipidová část membrán je směsí především fosfolipidů, glykolipidů, sfingomyelinu, kardiolipinu a cholesterolu, přičemž zastoupení těchto složek je v různých membránách velmi odlišné.
Značná část buněčných proteinů se vyskytuje pouze v membránách. Membránové proteiny zajišťují řadu specifických procesů spojených s transportními a rozpoznávacími funkcemi membrán (pumpy, nosiče, iontové kanály, receptory, enzymy apod.). Podle spojení s membránou se tyto proteiny rozdělují na integrální (vážou se k membráně poměrně silně hydrofobními vazbami; jsou zanořeny do dvojné vrstvy nebo ji překlenují) a periferní (vážou se k povrchu membrán slaběji, obvykle iontovými nebo vodíkovými vazbami k integrálním proteinům; často jsou v membráně uchyceny pomocí glykosyfosfatidylinositolové kotvy). Integrální proteiny jsou amfifilní, neboť části vystavené vodnému prostředí jsou polární, zatímco části uvnitř membrány jsou na svém povrchu hydrofobní. Není znám protein, který by byl v membráně zcela ukryt a nebyl tedy v interakci s vodným prostředím vně či uvnitř buňky. Základními atributy biomembrán jsou:
propustnost a řízený transmembránový transport látek;
dynamika membránových molekul;
elektrické vlastnosti.
MODEL BUNĚČNÉ MEMBRÁNY

Neurony i jiné buňky vytvářejí a udržují rozdílné koncentrace iontů na obou stranách plazmatické membrány. Jedná se o aktivní procesy, které používají specifické iontové pumpy. Výsledkem této činnosti je vznik membránového potenciálu, tedy napěťového rozdílu mezi vnitřní a vnější stranou membrány. Vnitřek buněk je negativní vůči vnějšku. Klidový membránový potenciál (stálý potenciál) dosahuje v různých buňkách -9 až -100 mV, v neuronech -40 až -90 mV (obvykle -70 mV).
Rychlost toku různých iontů přes membránu je dána jejich: 1. koncentračními gradienty mezi oběma stranami plazmatické membrány, 2. permeabilitou membrány pro jednotlivé ionty, 3. napěťovým rozdílem přes membránu. Pro každý typ iontu lze z rozdílu jeho koncentrací uvnitř a vně buňky určit rovnovážný potenciál (napětí potřebné k vyrovnání toku daného iontu přes membránu, tj. k rovnosti elektrických a difúzních sil pro daný iont) pomocí Nernstovy rovnice. Výsledný membránový potenciál na membráně, kterou může procházet více iontů, lze spočítat pomocí Goldmanovy, resp. Goldmanovy-Hodgkinovy-Katzovy rovnice, pokud známe koncentrace iontů a koeficienty permeability membrány pro jednotlivé ionty.
Při depolarizaci membrány je membránový potenciál méně negativní než klidový potenciál, při hyperpolarizaci je více negativní. K těmto změnám dochází transportem iontů přes membránu. Náboj potřebný pro vytvoření membránového potenciálu je velmi malý a odpovídá přibližně 10-20 molu monovalentního iontu na mm2 membrány. Vzhledem k tomu, že lipidová dvojná vrstva je dobrý elektrický izolátor a je tedy nepropustná pro nabité molekuly, jsou přesuny iontů umožněny především iontovými kanály a aktivním přenosem. Tok nábojů přes membránu se týká především iontů Na+, K+ a Cl-, další ionty jsou přítomny v mnohem nižších koncentracích. Většinu nitrobuněčných aniontů tvoří proteiny a jiné organické molekuly, pro něž je membrána téměř nepropustná. V klidu je permeabilita membrány pro Cl- a Na+ velmi nízká (kanály jsou většinou zavřené), ale permeabilita pro K+ je relativně vysoká (kanály jsou často otevřené). Klidový membránový potenciál je proto velmi blízký rovnovážnému potenciálu pro ionty K+, pouze je v důsledku nenulového toku iontů Na+ poněkud méně negativní. Klidový potenciál je tak veliký, aby vyrovnal toky různých iontů přes membránu (při jejich různých koncentračních gradientech a permeabilitách). Protože se klidový potenciál liší od rovnovážných potenciálů jednotlivých iontů, dochází k jejich průběžnému toku podle koncentračního gradientu, přičemž výsledný proud přes membránu je nulový. Membrána je tedy ve stavu ustáleném, ale nikoli rovnovážném. Koncentrační gradienty se musí udržovat aktivním transportem iontů.
Typické
koncentrace iontů v savčí buňce
|
iont |
konc.
uvnitř Xin |
konc.
vně Xex |
rovnovážný
potenciál Dy,
37°C |
|
|
(mM) |
(mM) |
(mV) |
|
K+ |
120 |
2 |
-109 |
|
Na+ |
10 |
122 |
+67 |
|
Ca2+ |
10-7 |
3 |
+230 |
|
Cl- |
4 |
120 |
-91 |
|
A- |
126 |
10 |
|
(Podle údajů z knihy: Atwood H.L., MacKay W.A.: Essentials of Neurophysiology. B.C. Decker Inc., Toronto, Philadelphia, 1989.)