symptomatická HIV infekce
akutní HIV infekce a 1/2 roku po ní (na 6-24 měsíců, v době ukončení by mělo být CD4+ >500/mm3, VL PCR HIV RNA <500/ml, dále ponechat bez terapie, sledovat)
asymptomatická HIV infekce - podle počtu CD4+ lymfocytů a virové nálože
| virová nálož HIV | počet CD4+ lymfocytů | ||
| PT PCR | ³350/ml | 200-350/ml | <200/ml |
| <50 000 - 100 000 | vyčkat | léčit podle progrese *) | léčit |
| >50 000 - 100 000 | léčit | léčit | léčit |
HIV infekce v graviditě (u žen bez antiretrovirové terapie - zidovudin v monoterapii v 2., event. 3. trimestru, při hlubokém imunodeficitu se zváží kombinovaná antiretrovirová terapie bezpečná pro plod, u žen s antiretrovirovou terapií se zváží rizika pro plod a v kombinované léčbě po event. úpravách pokračuje)
postexpoziční profylaxe po profesionální, event. neprofesionální expozici infekčnímu biologickému materiálu
Přihlíží se k dynamice, předpokladu dalšího vývoje, přání pacienta, pravděpodobné adherenci apod.
Argumenty pro časnou intervenci:Základní režimy
Odvozené režimy
Režimy s dalšími antiretrovirotiky
Základní kombinace nukleosidových inhibitorů revernzí transkriptázy: Z kombinací 2NRTI se volí obvykle ZDV+3TC, ZDV+ddI, d4T+ddI, d4T+3TC, popř. ZDV+ddC, ddI+3TC.
Režimy s inhibitory proteinázy (protease inhibitor-based regimens): Na horší adherenci se podílí vysoký počet tablet v denní dávce (např. nelfinavir, amprenavir) a nutnost podávat léky 3x denně s opatřeními v příjmu jídel a vody (např. indinavir nalačno a tekutiny, nelfinavir tučná jídla). Nevýhodou jsou nežádoucí účinky včetně skupinových metabolických nežádoucích účinků (lipodystrofie, hyperlipidémie, diabetes). Je nutné mít na paměti lékové interakce při podávání antihistaminik, benzodiazepinů, cisapridu, antiarytmik apod.
Režimy s inhibitory proteinázy vylepšené nízkodávkovaným ritonavirem (ritonavir-enhanced protease inhibitor-containing regimens): Ritonavir (RTV) podávaný v nízké dávce ("baby dose", obvykle 2x 100mg/d) inhibuje cytochromové enzymy (P450) a příznivě ovlivňuje farmakokinetiku ostatních IP: zvyšuje hladiny saquinaviru, indinaviru a lopinaviru (Kaletra již obsahuje kombinaci s RTV).
Režimy s nenukleosidovým inhibitorem revernzí transkriptázy (non-nucleoside reverse transcriptase inhibitor-based regimens): Zdůrazňuje se výborná účinnost a možnost vyhnout se podávání inhibitorů proteinázy. Nevýhodou je výskyt kožních reakcí (NVP, EFV), hepatotoxicita (NVP) a neuropsychické příznaky (EFV). Potenciální teratogenita EFV jej vyřazuje z léčby gravidních. NNRTI (NVP, EFV) mají tedy menší dlouhodobé nežádoucí účinky než IP, ale nástup rezistence je asi rychlejší.
Režimy s trojkombinací nukleosidových inhibitorů revernzí transkriptázy (triple-nucleoside reverse transcriptase inhibitor regimens): Výhodou je nízký počet tablet v denní dávce (celá trojkombinace v Triziviru - jen 2 tablety/den) a nízký potenciál k lékovým interakcím. Kombinace ZDV+3TC+ABV má horší efekt u pacientů s virovou náloží ³100 000 kopií/ml. Jinou nevýhodou je závažná hypersenzitivní reakce proti ABV (u 3% léčených) a mutace kódónu 184 (M184V) navozující zkříženou rezistenci k lamivudinu a abacaviru - 500-1000x snižuje citlivost k 3TC a 2-4x k ABV.
Režimy s kombinací nenukleosidového inhibitoru revernzí transkriptázy a inhibitoru proteinázy: Jako režim první volby se nezavádí pro vyšší riziko následné multirezistence proti antiretrovirotikům z více tříd (omezující další volbu) a více nežádoucích efektů podle použitých léků.
Hodnocení efektu léčby: Hodnotí se| Signifikantní změna | ||
| virová nálož | absolutní počet | ³3´ |
| logaritmus | ³0,5 log | |
| CD4+ lymfocyty | absolutní počet | >30% |
| relativní počet | >3% | |
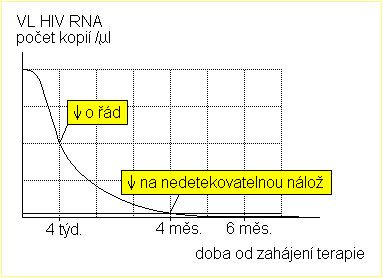
Žádoucí změny ve virové náloži:

Diskordance mezi trendy v počtu CD4+ lymfocytů a virové náloži: je nutno hodnotit individuálně.
Kritéria selhání léčby:
3-násobný a vyšší vzestup VL z úpatí hodnot (pokud nejde o přechodný vzestup při interkurentní infekci, očkování apod.).
Nedostatečná redukce VL: <0,5-0,75 log/ 4 týdny a <1 log/ 8 týdnů.
Nedosažení nedetekovatelné VL za 4-6 měsíců u pacientů s původně průměrnými hodnotami VL (<100000 kopií/ml).
Opakovaná detekce viru (zejména ve vyšších hodnotách >5000 kopií/ml) po počáteční nedetekovatelné hladině.
Kontinuálně klesající počet CD4+ lymfocytů.
Klinické zhoršení (za specifických okolností).
Příčiny selhání léčby:
non-adherence (nedodržování léčebného režimu)
špatná absorpce
poddávkování
rezistence HIV.
Vyšetření rezistence in vitro se indikuje po selhání léčby u pacientů, u nichž lze předpokládat dobrou adherenci.
Prostředky proti selhání léčby
Absorpci lze příznivě ovlivnit (1) lékovou formou (měkké tobolky saquinaviru a ritonaviru), (2) respektováním lékových interakcí (antacida a H2 antagonisté mohou snížit biologickou dostupnost některých antiretrovirotik), (3) načasováním podle příjmu jídla: užívání po jídle (resp. s jídly) vyžadují: většina inhibitorů proteinázy (kromě indinaviru a amprenaviru), užívání nalačno vyžadují: didanosin a indinavir, nevyžadují závislost na příjmu jídla: nukleosidové inhibitory reverzní transkriptázy kromě didanosinu, nenukleosidové inhibitory reverzní transkriptázy, amprenavir.
Poddávkování hrozí u pacientů s vysokou tělesnou hmotností a v důsledku nepříznivých lékových interakcí. V posouzení absorpce, ale i adherence by se mohlo v blízké budoucnosti uplatnit monitorování plazmatických hladin léků.
Individuální opatření k posílení adherence: Vysvětlit cíle léčby, předem informovat o vedlejších účincích, ujistit pacienta, že hledání alternativních režimů bude také přinášet těžkosti. Probrat s pacientem denní režim a nalézt činnosti, které poslouží jako stimuly pro braní léků. Poskytnout pacientovi i jednoduché doporučení písemnou formou. Využít technických pomůcek pro užívání léků (schránky s přihrádkami na léky, event. s budíkem, pagery atd.). Při návštěvě lékaře je třeba zhodnotit braní léků - např. počet vynechaných dávek za týden. Zapojit pokud možno přátele nebo členy rodiny do léčebného plánu. Při opakovaných návštěvách zdůrazňovat význam dodržování režimu a cíle terapie, posilovat důvěru ve zvolený léčebný režim.
Hlavními prostředky k oddálení nástupu rezistence jsou kombinovaná léčba a potlačení virové replikace k velmi nízkým hodnotám virové nálože (všemi výše uvedenými prostředky).
Změna léčby:Je indikována v případě selhání (kritéria 1-6), popř. nedostatečné adherence. Rovněž pacient s dobrou odpovědí na dvojkombinaci má být převeden na trojkombinaci (protože selhání léčby je pravděpodobnější než u pacienta na trojkombinaci).
Nový režimTeoretické důvody pro strukturované přerušení léčby (structured or supervised treatment interruption, STI):
Zatím chybí dostatek údajů pro vymezení indikací STI, proto není všeobecně doporučeno. Pacienti s STI musí být následně monitorováni.
| Skupina | Léčivo | Přípravek | Lékové formy |
| NRTI | zidovudin (ZDV), azidothymidin (AZT) | Retrovir | cap 100mg, cap 250mg, tab 300mg, sir 10mg/ml |
| Azitidin | tab 100mg | ||
| didanosin (ddI) | Videx | ctb 25mg, ctb 50mg, ctb 100mg, ctb 150mg, plv sol 100mg, plv sol 167mg, plv sol 250mg | |
| Videx EC | cap 400mg | ||
| zalcitabin (ddC) | Hivid | tab 0,375mg, tab 0,75mg, sir 0,1mg/ml | |
| stavudin (d4T) | Zerit | cap 30mg, cap 40mg, sir 1mg/ml | |
| lamivudin (3TC) | Epivir | tab 150mg, sol 10mg/ml | |
| abacavir (ABV) | Ziagen | tab 300mg, sol 20mg/ml | |
| ZDV + 3TC | Combivir | tab 300+150mg | |
| ZDV + 3TC + ABV | Trizivir | tab 300+150+300mg | |
| NtRTI | tenofovir | Viread | tab 300mg |
| NNRTI | nevirapin (NVR) | Viramune | tab 200mg, susp 10mg/ml |
| delavirdin (DLV) | Rescriptor | tab 100mg | |
| efavirenz (EFV) | Stocrin | cps 200mg | |
| Sustiva | cps 200mg | ||
| PI | saquinavir (SQV-hgc) | Invirase | cap 200mg |
| saquinavir (SQV-sgc) | Fortovase | cap 200mg | |
| ritonavir (RTV) | Norvir | cap 100mg, sol 80mg/ml | |
| indinavir (IDV) | Crixivan | cap 200mg, cap 400mg | |
| nelfinavir (NFV) | Viracept | tab 250mg, plv sol 50mg/g | |
| amprenavir (APV) | Agenerase | cap 150mg, sol 15mg/ml | |
| lopinavir/ ritonavir (LPV/r) | Kaletra | cap 133+33mg, sol (80+20)mg/ml | |
| Inhibitory fúze | enfuvirtid (T-20) | Fuzeon | inj 90mg |
Důležité interakce:
Některé souběžně podávané léky, které inhibují nebo indukují cytochromové enzymy, ovlivňují hladiny inhibitorů proteinázy: Inhibitory P450 (např. inhibitory proteinázy, zejména ritonavir a indinavir, makrolidy, azoly) jejich hladiny zvyšují. Induktory P450 (např. rifampicin, nevirapin) jejich hladiny snižují. Některé léky, které jsou metabolizovány cytochromovým systémem, jsou antiretrovirotiky farmakokineticky ovlivněny: Inhibitory proteinázy (které jsou inhibitory P450) zvyšují hladiny barbiturátů, benzodiazepinů, betablokátorů, klaritromycinu, rifampicinu, rifabutinu, event. jiných inhibitorů proteináz. Nevirapin (který je induktorem P450) snižuje hladinu barbiturátů, benzodiazepinů, betablokátorů, klaritromycinu, rifampicinu, rifabutinu, inhibitorů proteináz.
Dávkování:Nukleosidové inhibitory reverzní transkriptázy (NRTI)
Nukleotidové inhibitory reverzní transkriptázy (NtRTI)
Nenukleosidové inhibitory reverzní transkriptázy (NNRTI)
Inhibitory proteinázy (IP)
| NVP | EFV | DLV | SQV-hgc | SQV-sgc | |
| saquinavir (tvrdé tobolky) |
nedopor. | nedopor. | - | - | |
| saquinavir (měkké tobolky) |
3x 800mg | - | - | ||
| ritonavir |
2x 600mg | 2x 500-600mg | 2x 400mg | 2x 400mg | |
| indinavir |
3x 1000mg | 3x 1000mg | 3x 600mg | nedopor. | nedopor. |
| nelfinavir |
3x 750mg 2x 1250mg |
3x 750mg 2x 1250mg |
2x 1250mg | 3x 750mg 2x 1250mg |
3x 750mg 2x 1250mg |
| amprenavir |
3x 1200mg1) | 3x 800mg | 3x 800mg | ||
| lopinavir/ritonavir |
2x (533/133)mg | 2x (533/133)mg | 2x (400/100)mg |
| RTV | IDV | NFV | APV | LPV/r | |
| saquinavir (tvrdé tobolky) |
2x 400mg | nedopor. | |||
| saquinavir (měkké tobolky) |
2x 400mg | nedopor. | 3x 800mg - 2x 1200mg |
3x 800mg | 2x 800mg |
| ritonavir |
- | 2x 100-200mg2) 2x 400mg3) |
2x 400mg | 2x 100mg | - |
| indinavir |
2x 800mg4) 2x 400mg5) |
- | (2x 1200mg) | 2x 600mg | |
| nelfinavir |
2x 100-2006) | 3x 750mg 2x 1250mg |
- | 3x 750mg 2x 1250mg |
|
| amprenavir |
2x 600mg 1x 1200mg |
3x 800mg | 3x 800mg | - | 2x 750mg |
| lopinavir/ritonavir |
- | 2x (400/100)mg | 2x (400/100)mg | - |
1) 2x 1200mg pokud je současně přidán RTV, 2) při dávce IDV 2x 800mg, 3) při dávce IDV 2x 400mg, 4) při dávce RTV 2x 100-200mg, 5) při dávce RTV 2x 400mg, 6) při dávce RTV 2x 400mg
Inhibitory fúze